Фраза «редактирование генома впервые применили прямо в организме пациента» звучит громко, но буквально не сходится с историей технологии. In vivo CRISPR, когда редактор вводят сразу в тело, а не правят клетки в лаборатории, в клинику пришел раньше. Еще в 2020 году врачи впервые ввели такую терапию человеку, а дальше пошли системные попытки редактировать ткани уже после внутривенного введения.
Настоящая новость последних лет в другом. Врачи дошли не просто до in vivo CRISPR, а до персонализированной схемы под одного конкретного пациента. В статье NEJM описан младенец с тяжелым дефицитом CPS1, для которого за считаные месяцы собрали индивидуальную base-editing терапию с доставкой в печень. После двух инфузий авторы увидели ранний клинический эффект без серьезных нежелательных явлений на коротком горизонте наблюдения. Но сами исследователи честно пишут, что длинный контроль еще впереди. И вот здесь начинается самое важное.
Почему формулировка «впервые» сбивает с толку
Если под «впервые» понимать вообще любое редактирование генома прямо в теле человека, новость опоздала примерно на несколько лет. Если говорить о первом персонализированном in vivo лечении, собранном под одного ребенка с уникальной мутацией, формулировка уже гораздо ближе к правде.
Разница не словесная, а техническая. Ранние in vivo программы шли по более предсказуемым мишеням, где можно доставить редактор в печень или локально в глаз и измерить эффект по понятным биомаркерам. Персонализированная терапия для одного пациента намного сложнее. Нужно быстро подобрать направляющую РНК, проверить побочные попадания, собрать производственный процесс, пройти регуляторную оценку и сделать все вовремя, пока болезнь не ушла слишком далеко.
Чем in vivo редактирование отличается от классической генной терапии
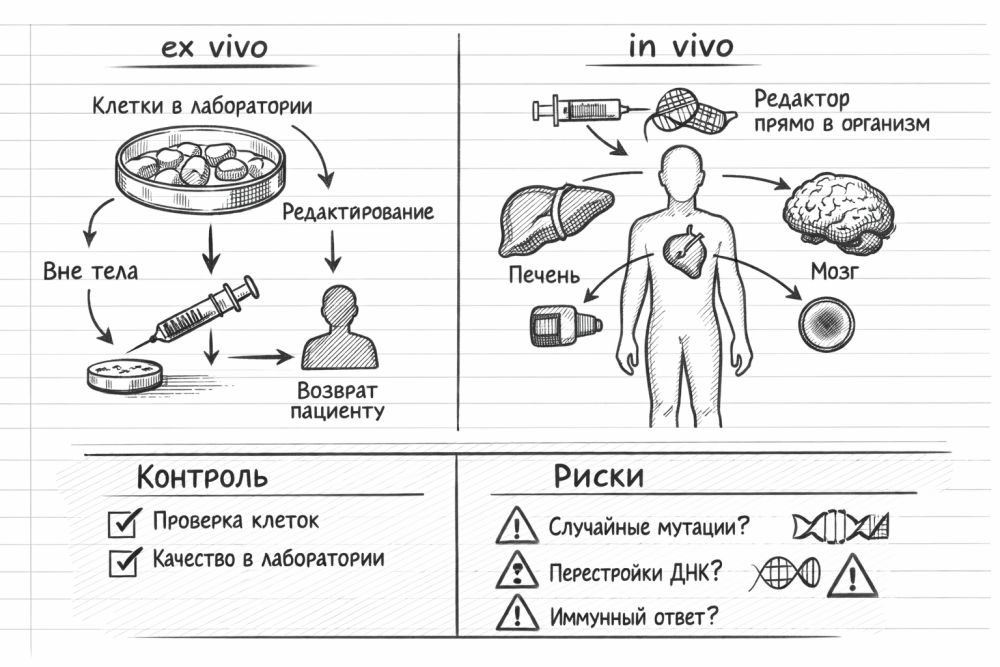
Многие смешивают три разные вещи. Классическая генная терапия часто не «чинит» исходный участок ДНК, а доставляет рабочую копию гена или меняет экспрессию. CRISPR-редактирование пытается вмешаться точнее и изменить сам геном в нужной точке. А дальше уже есть два режима: вне тела и внутри тела.
| Подход | Что делают | Сильная сторона | Главное ограничение |
|---|---|---|---|
| Классическая генная терапия | Доставляют рабочую генетическую конструкцию | Не всегда нужно резать исходную ДНК | Не любой дефект лечится простой «добавкой» гена |
| Редактирование ex vivo | Клетки забирают, редактируют в лаборатории, потом возвращают | Есть контроль качества клеточного продукта до введения | Сложно, дорого, подходит не для каждой ткани |
| Редактирование in vivo | Редактор вводят сразу пациенту, редактирование идет внутри тканей | Можно добраться до органов, которые трудно лечить вне тела | Меньше прямого контроля над тем, какие клетки и как именно изменились |
Поэтому тезис «in vivo CRISPR это просто следующий шаг после классической генной терапии» слишком прямолинейный. Иногда да. Иногда нет. Для болезней крови и костного мозга ex vivo подход пока во многих сценариях выглядит логичнее, потому что врачи видят и тестируют клетки до возврата пациенту. Для печени, глаза и ряда других тканей in vivo может оказаться удобнее и быстрее.
Почему первые победы чаще приходят в печени
Печень стала почти полигоном для in vivo редактирования не случайно. Липидные наночастицы хорошо доходят до печени, а многие болезни завязаны на белки, которые печень синтезирует и выбрасывает в кровь. Значит, эффект проще измерить. Если после введения препарата в крови устойчиво падает проблемный белок, исследователи быстро видят, что схема вообще сработала.
Есть и еще один неброский, но важный момент. Первые успешные программы часто не «исправляют» ген в классическом бытовом смысле, а выключают вредный участок или меняют одну букву в ДНК так, чтобы клетка перестала производить токсичный белок. С инженерной точки зрения такое вмешательство во многих случаях проще, чем полноценный ремонт сложной мутации во всех нужных клетках организма.
Почему персонализированный случай действительно тянет на большой рубеж
Случай с младенцем важен не только потому, что врачи впервые попробовали помочь очень конкретному ребенку. Главный смысл в том, что редактирование стало похоже не на единичный лабораторный трюк, а на платформу. Каркас терапии можно стандартизировать, а под конкретную мутацию менять направляющую часть и режим дозирования. Для редких болезней такой подход почти единственный шанс выйти из тупика, где пациентов слишком мало для длинной и дорогой классической разработки.
Но именно здесь прячется второй слой проблемы. Персонализированная медицина выглядит красиво в одном кейсе, а дальше упирается в производство, контроль, регуляторику и деньги. Нельзя просто сказать: «Раз сработало у одного ребенка, завтра так будем лечить сотни болезней». Между этими двумя фразами лежат годы стандартизации и огромный пласт работы, который обычно не попадает в заголовки.
Главный вопрос теперь не в том, работает ли CRISPR, а в том, насколько управляемы последствия
Переход от ex vivo к in vivo меняет саму философию контроля. При редактировании вне тела врач получает клеточный продукт, который можно измерять, сортировать, частично отбраковывать и проверять до инфузии. При редактировании внутри тела врач контролирует в первую очередь состав препарата и косвенные признаки результата после введения. Между точкой укола и реальным состоянием отдельных клеток появляется большая зона неопределенности.
Под «управляемостью» здесь скрывается сразу несколько разных вопросов. Куда именно попал редактор, сколько времени активные компоненты прожили в тканях, сколько клеток отредактировались как задумано, появились ли нежелательные изменения в похожих участках генома, возникли ли крупные перестройки ДНК, как отреагировала иммунная система, можно ли безопасно повторить введение, и что будет через год, три или десять лет.
Публичный разговор про CRISPR долго крутился вокруг off-target, то есть случайных попаданий мимо цели. Но картина уже шире. Обсуждают не только точечные промахи, но и крупные делеции, перестройки, транслокации и другие изменения структуры генома. Для клиники разница принципиальная. Небольшая побочная правка и большая хромосомная перестройка несут разный риск, а значит и разные требования к контролю.
Отдельный слой риска связан не с ножницами как таковыми, а с доставкой. Нужно доставить редактор в нужный орган, не расплескать по лишним тканям, не спровоцировать тяжелую иммунную реакцию и при этом сохранить достаточную эффективность. Именно поэтому в рекомендациях FDA отдельно разбирают разницу между ex vivo и in vivo подходами, длительность активности редактора, off-target-эффекты и риск хромосомных перестроек.
Где громкий тезис про «новую эру» пока не работает
Есть соблазн сделать простой вывод: раз редактор можно ввести сразу в организм, классическая генная терапия скоро уйдет в прошлое. Такой вывод преждевременен. Во многих сценариях добавление рабочей копии гена остается разумнее, чем редактирование исходного участка. Для некоторых болезней проблема не в одной букве ДНК, а в сложной регуляции, крупной делеции, потере целого фрагмента или в том, что поражены слишком разные типы клеток.
Не надо забывать и про биологию тканей. Печень удобна. Кроветворные клетки доступны для ex vivo работы. А вот мозг, мышцы, легкие и многие другие органы до сих пор остаются куда более трудной мишенью. Условно говоря, один яркий успех в печени еще не означает, что вся остальная медицина уже стоит в очереди на такой же сценарий.
Что будет дальше
Следующий этап почти наверняка пойдет по трем направлениям. Первое, улучшение доставки. Без более точного попадания в конкретные ткани разговор о массовом in vivo редактировании останется ограниченным. Второе, стандартизация платформы под редкие мутации, чтобы не собирать каждый препарат как кустарный проект. Третье, длинное наблюдение за пациентами, потому что настоящая цена точности выясняется не на седьмой неделе после инфузии, а через годы.
Если смотреть без лишнего восторга, медицина уже прошла точку, где CRISPR нужно доказывать как рабочую идею. Теперь CRISPR нужно доказывать как управляемую клиническую технологию. А это намного более жесткий экзамен.
Материал носит информационный характер и не заменяет консультацию врача. Решения о лечении, участии в клинических исследованиях и генетическом тестировании нужно принимать вместе с профильным врачом и медицинским генетиком.
Вывод
Главная новость не в том, что редактор генома «впервые» попал внутрь пациента. Главная новость в том, что in vivo CRISPR перестает быть демонстрацией возможности и начинает превращаться в медицинскую платформу. Персонализированный случай с младенцем показал, что технологию можно быстро собрать под конкретную болезнь и получить ранний эффект. Но каждый такой успех одновременно усиливает неудобный вопрос: как надежно контролировать необратимые изменения, когда редактирование происходит уже не в пробирке, а в живом организме. Именно на ответе на этот вопрос и будет решаться, останется ли in vivo CRISPR редким чудом или станет нормальной клинической практикой.
FAQ: in vivo CRISPR без путаницы
Редактирование внутри организма уже можно считать рутинной медициной?
Пока нет. Есть сильные клинические сигналы и очень важные кейсы, но для рутинной практики нужны длинные данные по безопасности, стандартизация производства и понятные регуляторные правила.
Почему ex vivo редактирование до сих пор не устарело?
Потому что ex vivo дает больше контроля. Клетки можно проверить до возврата пациенту. Для болезней крови и костного мозга такой подход пока во многих случаях остается более управляемым.
Что именно пугает врачей сильнее всего?
Не только классические off-target-попадания. Большую тревогу вызывают и крупные перестройки генома, иммунные реакции на доставку и ситуация, когда эффект оказался необратимым, а исправить последствия уже сложно.
Почему печень фигурирует в таких новостях чаще других органов?
Потому что в печень сравнительно удобно доставлять препарат, а результат часто можно быстро увидеть по анализам крови и по уровню белков, которые печень вырабатывает.
Заменит ли CRISPR всю классическую генную терапию?
Нет. Часть задач CRISPR решает лучше, часть хуже. В ближайшие годы правильнее ждать не замены одного подхода другим, а сосуществования нескольких терапевтических стратегий под разные болезни.


